Analyse de la vaccination contre la COVID-19 et l’incidence des cas au Canada

 Téléchargez cet article en format PDF
Téléchargez cet article en format PDFPublié par : L'Agence de la santé publique du Canada
Numéro : Volume 49-4, avril 2023 : La santé des enfants et la COVID-19
Date de publication : avril 2023
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 49-4, avril 2023 : La santé des enfants et la COVID-19
Surveillance
Analyse épidémiologique nationale portant sur l'association entre la vaccination contre la COVID-19 et l'incidence des cas de COVID-19 au Canada, de janvier à août 2021
Agence de la santé publique du Canada, équipes de la Surveillance de la COVID-19, des Couvertures vaccinales et systèmes d'information, du Programme de surveillance de l'efficacité des vaccins et de la Science des risques en santé publique/Laboratoire national de microbiologie1
Affiliation
1 Agence de la santé publique du Canada, Ottawa, ON
Correspondance
Citation proposée
Agence de la santé publique du Canada, équipes de la Surveillance de la COVID-19, des Couvertures vaccinales et systèmes d'information, du Programme de surveillance de l'efficacité des vaccins et de la Science des risques en santé publique/Laboratoire national de microbiologie. Analyse épidémiologique nationale portant sur l'association entre la vaccination contre la COVID-19 et l'incidence des cas de COVID-19 au Canada, de janvier à août 2021. Relevé des maladies transmissibles au Canada 2023;49(4):163–74. https://doi.org/10.14745/ccdr.v49i04a07f
Mots-clés : COVID-19, Canada, épidémiologie, surveillance, incidence, cas, vaccination
Résumé
Contexte : En décembre 2020, le Canada a lancé sa campagne de vaccination contre la maladie à coronavirus 2019 (COVID-19). Les Canadiens ont été vaccinés avec des intervalles de temps entre les doses, des vaccins et des calendriers de vaccination différents selon l'âge, le moment de la vaccination et la province ou le territoire. L'objectif de la présente étude est de décrire l'épidémiologie et l'association entre l'incidence des cas de COVID-19 après la vaccination, le temps écoulé depuis la fin de la série primaire, l'intervalle entre les doses et/ou l'ensemble de vaccins reçus, et la probabilité de développer des conséquences graves.
Méthodes : Les données nationales sur les cas de COVID-19 et les données sur la couverture vaccinale ont été extraites du Système national de surveillance de la COVID-19 et du Système canadien de surveillance de la couverture vaccinale contre la COVID-19. Les estimations de population de Statistique Canada ont servi de dénominateurs pour les taux et le nombre de personnes « pas entièrement vaccinées ». Deux modèles linéaires généralisés binomiaux ont été construits pour analyse.
Résultats : Au cours de la période couverte par l'analyse, les cas entièrement vaccinés (i.e. la série primaire complétée) (n = 17 206) étaient plus souvent des femmes et des personnes plus âgées, et présentaient moins d'issus graves comparativement aux cas qui n'étaient entièrement vaccinés (n = 615 999). La date d'épisode des cas entièrement vaccinés était le plus souvent observée dans les deux mois suivant la deuxième dose, et les catégories d'intervalle entre les doses de 29 à 49 et de 50 à 77 jours étaient les plus fréquentes. La probabilité de devenir un cas signalé de COVID-19 chez les personnes qui n'étaient pas entièrement vaccinées était plus élevée que chez celles qui étaient entièrement vaccinées. Les personnes recevant deux doses d'AstraZeneca et celles ayant des intervalles de temps les plus courts entre les doses présentaient des probabilités plus élevées de devenir des cas de COVID-19.
Conclusion : Les résultats issus des données des systèmes de surveillance nationaux au Canada confirment que le fait d'être entièrement vacciné contre la COVID-19, d'avoir un intervalle de temps plus long entre les doses et de recevoir un vaccin à base d'acide ribonucléique messager (ARNm) contre la COVID-19, comparativement à d'autres vaccins, réduit la probabilité de devenir un cas, selon les données de janvier à août 2021.
Introduction
Le 30 janvier 2020, l'Organisation mondiale de la Santé (OMS) a déclaré que l'éclosion du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) (maladie à coronavirus 2019; COVID-19) constituait une urgence de santé publique de portée internationale, et une pandémie a été déclarée le 11 mars 2020. Depuis, la pandémie a entraîné une morbidité, une mortalité et une menace importantes pour le bien-être général des Canadiens Note de bas de page 1 Note de bas de page 2. Les recommandations portaient surtout sur les actions individuelles et collectives, alors que le développement de vaccins sûrs et efficaces était en cours.
Le 14 décembre 2020, le Canada a amorcé sa campagne de vaccination contre l'infection à SRAS-CoV-2 après l'approbation des vaccins contre la COVID-19 Pfizer-BioNTech Comirnaty, Moderna Spikevax, AstraZeneca Vaxzevria et Janssen Jcovden (Johnson & Johnson) Note de bas de page 3. En raison des contraintes prévues en matière d'approvisionnement en vaccins, les premières doses de vaccins contre la COVID-19 ont été réservées en priorité aux populations clés. La campagne de vaccination a commencé auprès des résidents des établissements de soins de longue durée, des travailleurs de la santé et des adultes résidant dans les territoires ou vivant dans des collectivités éloignées et isolées. À mesure que l'approvisionnement en vaccins a changé, les recommandations du programme de vaccination contre la COVID-19 du Comité consultatif national de l'immunisation (CCNI) du Canada ont évolué. Durant la période couverte par le présent article (du 1er janvier au 31 août 2021, i.e. pendant les vagues des variants Alpha, Gamma et Delta) recevoir une deuxième dose d'un vaccin à deux doses (compléter la série primaire de vaccination) était recommandé pour offrir une meilleure protection à long terme contre la COVID-19 Note de bas de page 4. L'intervalle de temps recommandé entre les doses a été prolongé à quatre mois en mars 2021, alors qu'elle a été de 21 à 28 jours initialement; cependant, les intervalles différaient d'une province ou d'un territoire à l'autre en fonction de leurs stratégies de vaccination. L'admissibilité au vaccin s'est élargie et, en plus des recommandations visant à prolonger l'intervalle de temps entre les doses, tous les résidents canadiens âgés de 12 ans ou plus étaient admissibles à une première dose en mai 2021 Note de bas de page 5 Note de bas de page 6 Note de bas de page 7. En juin 2021, le CCNI a recommandé l'interchangeabilité des vaccins disponibles et l'utilisation préférentielle de vaccins à acide ribonucléique messager (ARNm) pour compléter la série primaire de vaccination en raison des préoccupations en matière de sécurité soulevées par l'utilisation du vaccin AstraZeneca (thrombose avec thrombocytopénie) Note de bas de page 6. Par conséquent, les Canadiens ont été vaccinés avec des intervalles de temps différents entre les doses, des vaccins et des calendriers de vaccination variés, selon l'âge, le moment de la vaccination et la province/le territoire de résidence. Une ligne de temps des recommandations au niveau national est disponible dans le document Matériel supplémentaire, figure S1.
Les vaccins contre la COVID-19 ont démontré une grande efficacité contre des complications graves de la maladie comme l'hospitalisation et des décès. Décrire les variations en matière de calendrier de vaccination et leur impact sur la dynamique de la transmission au Canada contribue au nombre grandissant de données probantes permettant de mieux définir l'efficacité à long terme du vaccin contre la COVID-19 ainsi que les futures politiques qui sous-tendent le développement des vaccins Note de bas de page 8 Note de bas de page 9 Note de bas de page 10 Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 15 Note de bas de page 16 Note de bas de page 17 Note de bas de page 18.
L'objectif du présent article est de décrire l'épidémiologie et d'explorer l'association entre l'incidence des cas de COVID-19 après la vaccination et le temps écoulé depuis l'achèvement de la série primaire. L'analyse inclut un résumé descriptif de la couverture vaccinale et des cas vaccinés, ainsi qu'une analyse par modélisation des cas signalés après la vaccination afin de déterminer si le temps écoulé depuis la dernière dose, l'intervalle entre les doses et/ou la combinaison de vaccins sont associés au fait de devenir un cas de COVID-19 ou de présenter des issues graves, après ajustement des covariables pertinentes.
Méthodes
Définitions
Selon les recommandations du CCNI au cours de la période d'analyse (du 1er janvier au 31 août 2021), les programmes de vaccination visaient en priorité l'administration des séries primaires de vaccins, signifiant que les personnes ayant une série primaire de vaccination complète étaient désignées comme « entièrement vaccinées ». Puisque les programmes de vaccination au Canada ont évolué au cours de la dernière moitié de 2021, avec le déploiement des doses additionnelles et de rappel, les définitions suivantes reflètent la vaccination jusqu'en août 2021 et se concentrent sur l'achèvement de la série primaire.
Pour cette analyse, le statut vaccinal des cas confirmés en laboratoire ne tenait compte que des vaccins approuvés par Santé Canada au cours de la période couverte par l'analyse (Pfizer-BioNTech Comirnaty [Pfizer]; Moderna Spikevax [Moderna]; AstraZeneca Vaxzevria ou COVISHIELD [AstraZeneca]) et a été définie selon les catégories suivantes :
- Cas « entièrement vaccinés » (i.e. cas avec une série primaire complète) : date de l'épisode 14 jours ou plus après la réception de la deuxième dose dans une série à deux doses. Dans le cadre de cette analyse, seules les séries primaires complètes sont incluses, puisque la période couverte par l'analyse est antérieure au déploiement de doses additionnelles et de rappel au Canada.
- Les cas « pas entièrement vaccinés » incluaient les scénarios suivants :
- Les cas non vaccinés comprenaient ceux qui n'avaient pas été vaccinés à la date de l'épisode.
- Les cas qui n'étaient pas encore protégés par la vaccination comprenaient ceux dont la date d'épisode était inférieure à 14 jours après la première dose de vaccin.
- Les cas partiellement vaccinés comprenaient ceux dont la date de l'épisode est survenue 14 jours ou plus après leur première dose de vaccin ou moins de 14 jours après leur deuxième dose de vaccin.
Le mois de la dernière dose désigne le mois où la deuxième dose d'un vaccin contre la COVID-19 à deux doses a été administrée. Il a été utilisé pour calculer le nombre de mois écoulés entre la dernière dose et l'infection (basée sur la date de l'épisode), appelé « mois depuis la dernière dose » dans la présente analyse.
La date de l'épisode a été utilisée pour classifier temporairement les cas confirmés et fait référence à la date de début des symptômes. Lorsque la date d'apparition des symptômes n'était pas disponible ou que le cas était asymptomatique, la date de l'épisode se rapporte soit à la date de collecte des échantillons de laboratoire, soit à la date de dépistage en laboratoire.
Sources de données
Les données sur la couverture vaccinale ont été tirées des registres de vaccination des provinces et territoires par l'entremise du Système canadien de surveillance de la couverture vaccinale contre la COVID-19. Les données agrégées par groupe d'âge de 10 ans, sexe, mois de la dernière dose, vaccins reçus (i.e. Pfizer-Pfizer, Moderna-Moderna, AstraZeneca-AstraZeneca, ARNm mixte, AstraZeneca-ARNm) et intervalle de temps entre les doses (de 0 à 28 jours, de 29 à 49 jours, de 50 à 77 jours, 78 jours ou plus) n'étaient disponibles que pour les personnes entièrement vaccinées en date du 14 août 2021. L'intervalle entre les doses reflétait les diverses recommandations à ce sujet publiées tout au long de la période d'intérêt (voir le Matériel supplémentaire, figure S1).
Les données nationales sur les cas de COVID-19 ont été extraites de l'Ensemble national de données sur les cas de COVID-19, qui comprend les renseignements détaillés sur les cas partagés par toutes les provinces et territoires et qui est maintenu par l'Agence de la santé publique du Canada (Agence). Pour cette analyse, les données de cas de COVID-19 comprenaient des données démographiques de base, les dates d'épisode, les issues graves, les vaccins reçus et la date de vaccination pour chaque dose administrée. Douze des 13 provinces et territoires (excluant le Québec) ont partagé les données de vaccination des cas pour la période couverte par l'analyse (du 1er janvier 2021 au 31 août 2021), et les données étaient extraites de l'ensemble national de données sur les cas de COVID-19 le 18 février 2022.
Le 1er juillet 2021, les estimations de population fournies par Statistique Canada pour les provinces et le Nunavut et les estimations de population fournies par les gouvernements du Yukon et des Territoires du Nord-Ouest ont servi de dénominateur pour les taux de couverture vaccinale et pour calculer le nombre de personnes non vaccinées Note de bas de page 19.
Analyse
L'analyse a porté sur les cas âgés de 12 ans ou plus confirmés en laboratoire, dont la date d'épisode est comprise entre le 1er janvier 2021 et le 31 août 2021 Note de bas de page 20.
Pour les analyses de modélisation statistique, les cas ont été regroupés par province ou territoire, groupe d'âge, sexe, statut vaccinal et le mois de l'épisode. Pour créer les dénominateurs, les données sur la couverture et les estimations de la population ont été utilisées pour déterminer le nombre de personnes, dans chaque province ou territoire, groupe d'âge, sexe et statut vaccinal, à risque de devenir un cas chaque mois. Les données sur les cas ont été liées aux dénominateurs de couverture pour calculer la proportion de personnes qui sont devenues un cas de COVID-19 dans chaque groupe agrégé. Les données sur la couverture comportaient des nombres discrets des personnes entièrement vaccinées, ce qui signifie que le statut vaccinal était classé comme étant soit entièrement vacciné, soit pas entièrement vacciné. Le nombre de personnes non vaccinées a été obtenu en soustrayant le nombre de personnes entièrement vaccinées des estimations de population de Statistique Canada. Pour les analyses par modélisation des personnes entièrement vaccinées, les cas ont été stratifiés et regroupés par série de vaccins, intervalle de temps entre les doses et nombre de mois depuis la dernière dose. Dans les données sur la couverture vaccinale, les personnes ont été considérées comme entièrement vaccinées le mois où ils ont achevé leur série primaire de vaccination. En ce qui concerne le nombre de mois écoulés depuis la dernière dose, une valeur de zéro mois a été assignée aux personnes entièrement vaccinées dont la série primaire achevait le mois en question.
Les cas pour lesquels la date de vaccination, le nom du vaccin, les données démographiques (âge et sexe) ou la date de l'épisode étaient manquants ou non valides ont été exclus de l'analyse (moins de 0,5 % des cas). Afin d'aligner les données sur les cas de COVID-19 avec l'ensemble de données sur la couverture vaccinale, les cas qui ont reçu plus de deux doses d'un vaccin contre la COVID-19, le vaccin Janssen contre la COVID-19, ou un vaccin contre la COVID-19 non autorisé par Santé Canada ont été exclus, de même pour les cas entièrement vaccinés qui ont complété leur série primaire après le 14 août 2021.
Modèles statistiques
Deux modèles linéaires généralisés binomiaux ont été construits pour évaluer les associations entre la vaccination contre la COVID-19, les caractéristiques de la vaccination (i.e. les vaccins reçus, l'intervalle de temps entre les doses et le temps depuis la dernière dose) et l'incidence de la COVID-19. Dans chaque modèle, la principale variable dépendante était la proportion de personnes qui sont devenues des cas de COVID-19 dans un mois, parmi leur cohorte respective. Le nombre total de personnes dans chaque groupe agrégé a été inclus comme poids dans les modèles, et toutes les variables prédictives ont été incluses comme variables catégoriques. Les provinces de l'Atlantique (Terre-Neuve-et-Labrador, Nouveau-Brunswick, Île-du-Prince-Édouard et Nouvelle-Écosse) ont été regroupées sous la région « Atlantique », tandis que tous les territoires ont été exclus en raison du faible nombre de cas.
Un modèle principal (modèle 1) a été ajusté aux données regroupées selon la province ou région, le groupe d'âge, le sexe, le mois de l'épisode et le statut vaccinal. Un deuxième modèle (modèle 2) a été ajusté aux groupes entièrement vaccinés, regroupés par province ou région, groupe d'âge, sexe, mois de l'épisode, série de vaccins reçus, intervalle de temps entre les doses et mois de la dernière dose. Les variables utilisées pour regrouper les données ont été incluses comme variables prédictives dans chaque modèle.
À l'aide des deux modèles d'ajustement, les effets prédits de chaque niveau de chaque variable ont été calculés. Lors du calcul de l'effet d'un niveau, tous les autres niveaux variables ont été contrôlés à leur valeur moyenne. Pour chaque niveau, des estimations ponctuelles et des intervalles de confiance de 95 % ont été générés pour déterminer la probabilité qu'une personne devienne un cas de COVID-19 signalé. Les valeurs p au niveau des variables ont été calculées pour évaluer la signification statistique de toutes les variables prédictives.
Le nettoyage, la manipulation et la visualisation des données ont été effectués dans Excel MS Office et SAS V9.4. Les analyses statistiques ont été effectuées dans R version 4.0.2.
Résultats
En date du 14 août 2021, 72 % (n = 24 209 666) des 12 ans et plus étaient entièrement vaccinés au Canada. Parmi ces personnes, 9 % ont complété leur série primaire entre janvier et mai 2021 et 84 % ont complété leur série primaire entre juin et juillet 2021, compte tenu de la campagne de vaccination au Canada. Parmi les personnes de 50 ans ou plus entièrement vaccinées, la plupart ont terminé leur série en juin 2021 (allant de 44 % chez les 50 à 59 ans à 67 % chez les 70 à 79 ans). La majorité des plus jeunes groupes d'âge ayant complété leur série primaire l'ont fait en juillet 2021 (allant de 50 % chez les 40 à 49 ans à 67 % chez les 12 à 17 ans) (figure 1).
(A)

Figure 1A - Équivalent textuel
| Mois de la dernière dose | 12–17 | 18–29 | 30–39 | 40–49 | 50–59 | 60–69 | 70–79 | 80+ | Couverture vaccinale (12+) |
|---|---|---|---|---|---|---|---|---|---|
| Janvier 2021 | 0,02 % | 0,49 % | 0,70 % | 0,73 % | 0,67 % | 0,38 % | 0,18 % | 0,56 % | 0 % |
| Février 2021 | 0,05 % | 1,31 % | 1,79 % | 1,83 % | 1,73 % | 1,30 % | 1,50 % | 7,26 % | 2 % |
| Mars 2021 | 0,02 % | 0,47 % | 0,56 % | 0,55 % | 0,59 % | 0,70 % | 0,79 % | 3,51 % | 2 % |
| Avril 2021 | 0,06 % | 0,92 % | 1,05 % | 1,08 % | 1,16 % | 1,11 % | 4,09 % | 8,26 % | 4 % |
| Mai 2021 | 0,27 % | 3,35 % | 3,83 % | 3,97 % | 4,19 % | 4,69 % | 5,64 % | 11,70 % | 7 % |
| Juin 2021 | 11,94 % | 26,47 % | 30,33 % | 35,55 % | 43,62 % | 57,90 % | 67,08 % | 54,49 % | 37 % |
| Juillet 2021 | 67,43 % | 55,47 % | 52,93 % | 49,62 % | 43,02 % | 30,55 % | 18,88 % | 13,15 % | 67 % |
| Août 2021 | 20,22 % | 11,51 % | 8,81 % | 6,67 % | 5,02 % | 3,37 % | 1,84 % | 1,07 % | 72 % |
(B)
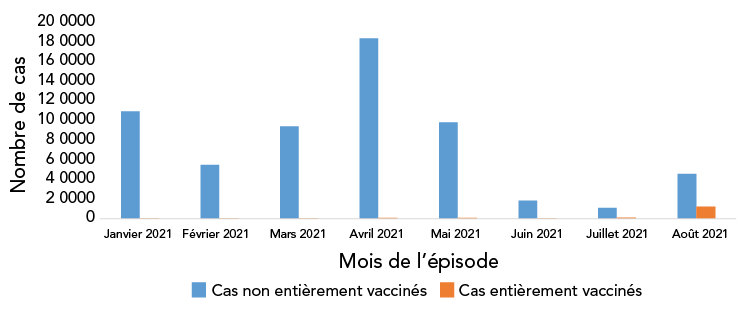
Figure 1B - Équivalent textuel
| Mois de l'épisode | Cas non entièrement vaccinés | Cas entièrement vaccinés |
|---|---|---|
| Janvier 2021 | 109 387 | 6 |
| Février 2021 | 54 899 | 87 |
| Mars 2021 | 94 244 | 319 |
| Avril 2021 | 183 085 | 1 022 |
| Mai 2021 | 98 459 | 1 119 |
| Juin 2021 | 18 782 | 574 |
| Juillet 2021 | 11 411 | 1 437 |
| Août 2021 | 45 752 | 12 642 |
Parmi les provinces et les territoires, les résidents des territoires ont complété leur série primaire plus tôt que dans les provinces. Parmi les territoires, 62 % à 75 % des personnes de 12 ans ou plus ont terminé leur série primaire en avril 2021, comparativement à 2 % à 11 % dans les provinces (Matériel supplémentaire, figure S2).
Il y a eu 633 205 cas confirmés de COVID-19 signalés à l'Ensemble national de données de cas de COVID-19 dont la date d'épisode se situait entre le 1er janvier 2021 et le 31 août 2021, et qui répondaient aux critères d'inclusion de l'analyse. De ce nombre, 17 206 (2,8 %) cas étaient entièrement vaccinés à la date de l'épisode, comparativement à 615 999 (97,2 %) qui n'étaient pas entièrement vaccinés à la date de l'épisode (tableau 1). Voir la figure S3 pour la description de la population de cas pour analyse. Comme les campagnes de vaccination ont priorisé les populations clés, y compris les résidents des établissements de soins de longue durée, les travailleurs de la santé et les adultes âgés, en diminuant l'âge d'admissibilité au fil du temps, les cas entièrement vaccinés étaient plus âgés (âge médian de 45 ans comparativement à 37 ans chez les cas non vaccinés) et plus souvent des femmes comparativement aux cas non vaccinés. La majorité des cas non vaccinés sont survenus en avril 2021 (n = 183 085); 29,7 %), alors que la plupart des cas entièrement vaccinés sont survenus en août 2021 (n = 12 642; 73,5 %; figure 1). Il y a eu moins d'hospitalisations et de décès signalés dans les cas entièrement vaccinés que dans les cas non vaccinés pendant la période couverte par l'analyse (tableau 1). Voir le tableau S1 pour le nombre et le pourcentage des 12 ans et plus qui étaient entièrement vaccinés selon la province ou le territoire, le groupe d'âge et le sexe au Canada.
| Caractéristiques | Total (n = 633 205) | |||||
|---|---|---|---|---|---|---|
| Cas « non entièrement vaccinés » (n = 615 999) | Cas « entièrement vaccinés » (n = 17 206) | Total de cas, n | ||||
| n | % | n | % | |||
| Groupe d'âge (en années) | ||||||
| 12 à 17 | 49 733 | 8,1 % | 275 | 1,6 % | 50 008 | |
| 18 à 29 | 171 734 | 27,9 % | 3 533 | 20,5 % | 175 267 | |
| 30 à 39 | 121 332 | 19,7 % | 3 194 | 18,6 % | 124 526 | |
| 40 à 49 | 98 259 | 16,0 % | 2 829 | 16,4 % | 101 088 | |
| 50 à 59 | 85 091 | 13,8 % | 2 504 | 14,6 % | 87 595 | |
| 60 à 69 | 50 873 | 8,3 % | 2 136 | 12,4 % | 53 009 | |
| 70 à 79 | 23 039 | 3,7 % | 1 220 | 7,1 % | 24 259 | |
| 80 ou plus | 15 938 | 2,6 % | 1 515 | 8,8 % | 17 453 | |
| Sexe | ||||||
| Homme | 314 935 | 51,1 % | 7 185 | 41,8 % | 322 120 | |
| Femme | 301 064 | 48,9 % | 10 021 | 58,2 % | 311 085 | |
| Mois de l'épisode | ||||||
| Janvier | 109 387 | 17,8 % | 6 | 0,0 % | 109 393 | |
| Février | 54 899 | 8,9 % | 87 | 0,5 % | 54 986 | |
| Mars | 94 244 | 15,3 % | 319 | 1,8 % | 94 543 | |
| Avril | 183 085 | 29,7 % | 1 022 | 5,9 % | 184 107 | |
| Mai | 98 459 | 16,0 % | 1 119 | 6,5 % | 99 578 | |
| Juin | 18 782 | 3,0 % | 574 | 3,3 % | 19 356 | |
| Juillet | 11 411 | 1,8 % | 1 437 | 8,4 % | 12 848 | |
| Août | 45 752 | 7,4 % | 12 642 | 73,5 % | 58 394 | |
| Province ou territoire | ||||||
| Colombie-Britannique | 98 201 | 15,9 % | 3 575 | 20,8 % | 101 776 | |
| Alberta | 125 909 | 20,4 % | 5 425 | 31,5 % | 131 334 | |
| Saskatchewan | 32 072 | 5,2 % | 1 330 | 7,7 % | 33 402 | |
| Manitoba | 26 296 | 4,3 % | 607 | 3,5 % | 26 903 | |
| Ontario | 326 645 | 53,0 % | 5 923 | 34,4 % | 332 568 | |
| Atlantique | 6 009 | 1,0 % | 142 | 0,8 % | 6 151 | |
| Nouveau-Brunswick | 1 115 | 0,2 % | 37 | 0,2 % | 1 152 | |
| Nouvelle-Écosse | 3 783 | 0,6 % | 72 | 0,4 % | 3 855 | |
| Terre-Neuve-et-Labrador | 993 | 0,2 % | 25 | 0,1 % | 1 018 | |
| Île-du-Prince-Édouard | 118 | 0,0 % | 8 | 0,0 % | 126 | |
| Territoires | 867 | 0,1 % | 204 | 1,2 % | 1 071 | |
| Yukon | 441 | 0,1 % | 88 | 0,5 % | 529 | |
| Territoires du Nord-Ouest | 213 | 0,0 % | 111 | 0,6 % | 324 | |
| Nunavut | 213 | 0,0 % | 5 | 0,0 % | 218 | |
| Conséquence grave | ||||||
| Hospitalisation | 33 523 | 5,4 % | 809 | 4,7 % | 34 332 | |
| Mortalité | 6 353 | 1,0 % | 272 | 1,6 % | 6 625 | |
| Nombre de mois depuis la dernière doseNote de bas de page a | ||||||
| 0 mois | s.o. | s.o. | 449 | 2,6 % | 449 | |
| 1 mois | s.o. | s.o. | 4 564 | 26,5 % | 4 564 | |
| 2 mois | s.o. | s.o. | 7 002 | 40,7 % | 7 002 | |
| 3 mois | s.o. | s.o. | 1 994 | 11,6 % | 1 994 | |
| 4 mois | s.o. | s.o. | 1 173 | 6,8 % | 1 173 | |
| 5 mois | s.o. | s.o. | 623 | 3,6 % | 623 | |
| 6 mois | s.o. | s.o. | 1 190 | 6,9 % | 1,19 | |
| 7 mois | s.o. | s.o. | 211 | 1,2 % | 211 | |
| Intervalle entre les deux dosesNote de bas de page a | ||||||
| 0 à 28 jours | s.o. | s.o. | 3 192 | 18,6 % | 3 192 | |
| 29 à 49 jours | s.o. | s.o. | 6 313 | 36,7 % | 6 313 | |
| 55 à 77 jours | s.o. | s.o. | 5 967 | 34,7 % | 5 967 | |
| 78 jours ou plus | s.o. | s.o. | 1 734 | 10,1 % | 1 734 | |
|
||||||
La série de vaccins reçus pour compléter la série primaire la plus commune était le Pfizer-Pfizer (63,2 %), suivi du Moderna-Moderna (17,5 %). Parmi les cas entièrement vaccinés, la majorité a reçu deux doses du vaccin Pfizer-Pfizer (n = 11 608; 67,5 %). Les cas entièrement vaccinés étaient plus fréquents lorsque la date d'épisode correspondait à deux mois suivant la deuxième dose reçue pour compléter la série primaire de vaccination (n = 7 002; 40,7 %), et les intervalles entre les doses de 29 à 49 jours (n = 6 313; 36,7 %) et de 50 à 77 jours (n = 5 967; 34,7 %) étaient les plus fréquents. Voir le tableau S2 pour le nombre et le pourcentage de personnes de 12 ans ou plus qui ont été entièrement vaccinées par intervalle entre les doses, par mois de la dernière dose et par série de vaccins reçus, au Canada en date du 14 août 2021. À partir du modèle 1, les valeurs p au niveau des variables ont indiqué une signification statistique à p < 0,001 pour toutes les variables prédictives, sauf pour le sexe (p = 0,18; Matériel supplémentaire, tableau S3; voir la figure S4 pour les effets prédits du sexe). Les effets prédits ont démontré que la probabilité de devenir un cas signalé de COVID-19 était plus élevée chez les personnes non vaccinées que chez les personnes entièrement vaccinées, après ajustement pour les provinces, l'âge, le sexe et le mois de l'épisode (figure 2). La probabilité de devenir un cas signalé de COVID-19 chez une personne non vaccinée était estimée à 0,204 % (IC à 95 %, 0,203–0,206; Matériel supplémentaire, tableau S3). Comparativement, la probabilité estimée pour une personne entièrement vaccinée était de 0,023 % (IC à 95 %, 0,023–0,024).

Figure 2 - Équivalent textuel
L'effet des covariables incluses dans le modèle 1 sur la probabilité prédite qu'une personne devienne un cas signalé de COVID-19. Les points et les lignes verticales montrent l'effet et l'intervalle de prédiction de 95 %, lorsqu'ils sont visibles. Les covariables pour lesquelles l'effet n'était pas significativement différent selon les différentes catégories ne sont pas affichées (la variable du sexe uniquement).
À partir du modèle 2, les valeurs p au niveau des variables ont indiqué une signification statistique à p < 0,001 pour toutes les variables prédictives, sauf le sexe (p = 0,22; Matériel supplémentaire, tableau S4). Les effets prédits ont démontré qu'après avoir pris en compte les variables prédictives, les personnes entièrement vaccinées recevant deux doses d'AstraZeneca et les personnes entièrement vaccinées avec l'intervalle de temps le plus court entre les doses (de 0 à 28 jours) présentaient des probabilités plus élevées de devenir un cas signalé de COVID-19, comparativement aux personnes ayant reçu d'autres vaccins et à celles avec intervalles de temps entre les doses différents, respectivement (figure 3). Dans l'ensemble, on peut observer la probabilité croissante de devenir un cas signalé, à mesure que le temps écoulé depuis l'achèvement de la série primaire soit passé de zéro à six mois (figure 3).

Figure 3 - Équivalent textuel
L'effet des covariables incluses dans le modèle 2 sur la probabilité prédite que des personnes entièrement vaccinées deviennent un cas signalé de COVID-19. Les points et les lignes verticales montrent l'effet et l'intervalle de prédiction de 95 %, lorsqu'ils sont visibles. Les covariables pour lesquelles l'effet n'était pas significativement différent selon les différentes catégories ne sont pas affichées (la variable du sexe uniquement).
Discussion
Principaux résultats
À l'échelle nationale, les résultats démontrent que la majorité les 12 ans et plus entièrement vaccinés ont complété la série primaire entre juin et juillet 2021, la plupart des 50 ans et plus ayant complété leur série primaire en juin et la plupart des 12 à 49 ans l'ont fait en juillet. De plus, les cas qui résident dans les territoires ont complété la série primaire plus tôt comparativement à ceux des provinces. Ces observations coïncident avec la façon dont le vaccin a été déployé au Canada qui visait initialement les groupes d'âge plus âgés, les populations à risque et les adultes résidant dans les territoires ou vivant dans des collectivités éloignées et isolées. Avec l'admissibilité au vaccin élargie avec le temps, les résidents canadiens âgés de 12 ans ou plus n'étaient admissibles à une première dose qu'en mai 2021 Note de bas de page 5. Les résultats ont montré que la majorité des cas non vaccinés étaient survenus en avril 2021. Cela concorde avec la troisième vague de cas de COVID-19 entrainé par le variant Alpha, ainsi qu'avec la plus faible couverture vaccinale chez les 12 ans ou plus (seuls 4 % de ce groupe d'âge étaient entièrement vaccinés à ce moment-là). La première dose de vaccin était en train d'être déployée et l'admissibilité était en pleine expansion, ce qui a résulté un plus faible nombre de personnes protégées contre la COVID-19 à ce moment-là Note de bas de page 21 Note de bas de page 22 Note de bas de page 23. Parmi les cas qui répondaient aux critères d'analyse, les personnes non vaccinées avaient une probabilité plus élevée de devenir un cas que celles qui avaient été vaccinées, ce qui est conforme aux analyses menées à l'international Note de bas de page 15 Note de bas de page 24 Note de bas de page 25. Les cas entièrement vaccinés étaient plus susceptibles d'être des femmes et plus âgés comparativement aux cas qui n'étaient pas entièrement vaccinés, puisque l'admissibilité au vaccin visait initialement les personnes plus âgées et les personnes travaillant dans des établissements de soins de santé, où les femmes sont plus nombreuses Note de bas de page 26 Note de bas de page 27.
Cette analyse a permis d'étudier plus en détail les facteurs en lien avec l'administration vaccin et de déterminer si le temps écoulé depuis la dernière dose, l'intervalle de temps entre les doses ou la combinaison de vaccins sont associés au fait de devenir un cas de COVID-19. Parmi les personnes entièrement vaccinées, celles qui ont un intervalle plus court entre les doses (de 0 à 28 jours), celles ayant reçu deux doses d'AstraZeneca et celles ayant un intervalle de temps accru depuis la dernière dose, de zéro à six mois, ont une probabilité plus élevée de devenir un cas de COVID-19. Les personnes qui ont été vaccinées sept mois après leur dernière dose avaient une probabilité plus faible de devenir un cas; cependant, les résultats doivent être interprétés avec prudence, car la cohorte de personnes admissibles à devenir un cas sept mois après la fin de la série était faible (n = 211, août 2021), en raison de période couverte par l'analyse.
Comparaison
La littérature suggère que l'âge Note de bas de page 6 Note de bas de page 9 Note de bas de page 10 Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 16 Note de bas de page 24 Note de bas de page 25 Note de bas de page 28 Note de bas de page 29 Note de bas de page 30 Note de bas de page 31, le type de vaccins utilisés Note de bas de page 6 Note de bas de page 10 Note de bas de page 12 Note de bas de page 14 Note de bas de page 16 Note de bas de page 24 Note de bas de page 25 Note de bas de page 29 Note de bas de page 31 Note de bas de page 32, l'intervalle de temps entre les doses, le temps écoulé depuis la dernière dose Note de bas de page 6 Note de bas de page 9 Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 15 Note de bas de page 16 Note de bas de page 18 Note de bas de page 25 Note de bas de page 28 Note de bas de page 29 Note de bas de page 30 Note de bas de page 31 Note de bas de page 32 Note de bas de page 33 Note de bas de page 34, le statut vaccinal Note de bas de page 8 Note de bas de page 12 Note de bas de page 24 Note de bas de page 25 Note de bas de page 29 Note de bas de page 31 et la prédominance de variants émergents et en évolution Note de bas de page 9 Note de bas de page 15 Note de bas de page 25 Note de bas de page 31 Note de bas de page 33 peuvent avoir une incidence sur la durée de protection contre la COVID-19 et sa gravité Note de bas de page 6 Note de bas de page 8 Note de bas de page 9 Note de bas de page 10 Note de bas de page 11 Note de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 15 Note de bas de page 16. Cette analyse au niveau national est conforme aux analyses effectuées à l'échelle interprovinciale et internationale, soutenant que l'efficacité du vaccin contre l'infection a diminué dans tous les groupes d'âge, un à six mois après la vaccination complète Note de bas de page 12. Les résultats suggèrent que des diminutions de l'efficacité du vaccin pourraient être en partie dues à la diminution de l'immunité, comme le démontre une étude menée en Israël, où les personnes qui ont complété leur série primaire de vaccination en janvier et février 2021 avaient un risque 2,26 fois plus élevé de développer la COVID-19 par rapport à celles qui ont complété leur série primaire en mars et avril 2021 Note de bas de page 18. Une tendance similaire a été observée dans une étude menée en Angleterre, où une plus grande diminution de l'efficacité vaccinale était observée chez les adultes plus âgés, spécifiquement chez les 65 ans ou plus et chez ceux qui étaient cliniquement vulnérables Note de bas de page 6. Des études canadiennes menées en Ontario, en Colombie-Britannique et au Québec ont montré que l'efficacité vaccinale contre l'infection était plus élevée avec un ensemble de vaccins contenant un vaccin à ARNm comparativement à deux doses du vaccin AstraZeneca Vaxzevria Note de bas de page 31 Note de bas de page 35. En ce qui concerne l'intervalle de temps entre les doses, des études menées aux États-Unis et en Israël ont montré que le temps écoulé entre la dernière dose et le moment où l'on devient un cas était significativement plus long chez ceux qui avaient un intervalle de temps plus long entre les doses comparativement à ceux qui avaient un intervalle entre les doses inférieur à 90 jours, l'atténuation augmentant par mois Note de bas de page 28 Note de bas de page 33.
Forces et limites
Compte tenu du déploiement unique de la vaccination au Canada, il s'agit de la première analyse à évaluer à l'échelle nationale les liens entre le statut vaccinal, les caractéristiques de vaccination (i.e. les vaccins reçus, l'intervalle de temps entre les doses et le temps depuis la dernière dose) et l'incidence des cas en fonction de ces facteurs. Cette analyse a une forte représentativité de l'ensemble du Canada, avec 12 des 13 provinces et territoires ayant fourni des renseignements sur la vaccination des cas de COVID-19 et avec toutes les provinces et tous les territoires ayant fourni des données sur la couverture vaccinale; néanmoins, la variabilité des rapports entre les provinces et les territoires peut avoir une incidence sur l'interprétation. Cette analyse comporte plusieurs limites, dont l'une concerne le fait que les données de vaccination des cas n'étaient pas disponibles pour toutes les provinces et tous les territoires, ce qui peut entraîner une surgénéralisation des résultats au niveau national. L'expansion des critères d'admissibilité au vaccin au Canada au cours de la période couverte par l'analyse (de janvier à août 2021) a également présenté des défis contextuels supplémentaires pour l'interprétation des résultats, particulièrement dus à une représentativité variable de la population canadienne au cours de la période d'analyse.
Deuxièmement, cette analyse a été limitée par les données de couverture vaccinale qui n'incluaient pas le nombre de personnes entièrement vaccinées selon le mois de la dernière dose. Ainsi, seules deux catégories de statut vaccinal ont pu être analysées, soit les personnes entièrement vaccinées et celles qui n'étaient pas entièrement vaccinées, puisque la granularité des données a été estompée par dernier groupe de classification qui est non conventionnel. Comme la vaccination partielle a démontré qu'elle réduisait le risque d'infection par le SRAS-CoV-2, l'inclusion de personnes partiellement vaccinées dans le groupe non vacciné peut avoir une incidence sur les effets estimés lors de la comparaison selon le statut vaccinal Note de bas de page 36 Note de bas de page 37 Note de bas de page 38. Les dénombrements par mois de la dernière dose dans les données de couverture vaccinale n'ont pas permis de tenir compte de façon précise des 14 jours nécessaires pour obtenir une protection induite par la série primaire de vaccination. Les personnes étaient considérées comme entièrement vaccinées le mois où elles ont reçu leur dernière dose, ce qui a surestimé artificiellement les estimations de la couverture vaccinale pour la série primaire complétée pour le mois en question (zéro mois depuis la dernière dose) et dans une moindre mesure le mois suivant.
De plus, cette analyse n'a porté que sur les cas survenus durant la période de huit mois qui a suivi le début de la vaccination au Canada, ce qui a limité la généralisation et la taille des groupes de couverture entièrement vaccinés avec des mois plus longs depuis la dernière dose. La période d'analyse limitée a également empêché l'évaluation des cas graves, car les hospitalisations chez les cas vaccinés étaient peu fréquentes (n = 809), ce qui n'était pas suffisant pour la stratification requise pour la construction du modèle.
Enfin, cette analyse n'a pas examiné explicitement l'impact des mesures de santé publique ni celui des variants en raison du nombre limité de cas pour lesquels le séquençage complet du génome était disponible. L'analyse portait sur la période concomitante aux vagues Alpha et Delta. Celles-ci n'ont pas été identifiées de façon explicite comme modificateurs d'effet sur les infections survenues suivant la vaccination ni sur l'efficacité vaccinale, puisque plusieurs études ont suggéré que l'efficacité vaccinale et le fardeau causé par le virus étaient réduits avec la circulation du variant Delta Note de bas de page 6 Note de bas de page 11 Note de bas de page 25 Note de bas de page 30.
Interprétation et généralisation
Les provinces incluses dans les modèles linéaires généralisés représentent 77 % de la population canadienne (9 provinces/territoires sur 13) et les provinces et territoires inclus dans l'analyse descriptive représentent 78 % de la population canadienne (12 provinces/territoires sur 13). Le programme de vaccination et la disponibilité du vaccin variaient selon les provinces et les territoires et au fil du temps; par conséquent, l'interprétation au niveau national devrait être faite avec prudence.
Conclusion
Les résultats obtenus à l'aide des systèmes de surveillance nationaux au Canada soulignent que la série primaire de vaccination contre la COVID-19 complète, un intervalle de temps plus long entre les doses et la série de vaccins contre la COVID-19 incluant un vaccin à ARNm réduisent la probabilité subséquente de devenir un cas de COVID-19. Les analyses au niveau national éclairent les lignes directrices sur les doses de rappel et contribuent à l'ensemble grandissant de données probantes sur la performance du vaccin contre la COVID-19 et sur les recommandations en matière de vaccination. D'autres analyses au niveau national portant sur les variants, les cas graves et les mesures de santé publique pourraient renforcer la recherche et les recommandations sur l'efficacité vaccinale.
Déclaration des auteurs
S. B. — Responsable de l'analyse de modèle, traitement des données, analyse officielle, révision et édition
B. H. M. F. — Analyse officielle des ensembles de données sur la couverture vaccinale, révision et édition
J. R. — Conceptualisation et analyse des ensembles de données sur la couverture vaccinale et révision
S. M. — Analyse officielle de l'ensemble de données de cas, révision et édition
F. B. — Analyse officielle de l'ensemble de données de cas
J. M. — Ébauche originale, révision et édition
N. L. — Responsable du manuscrit, révision et édition
M. L. — Orientation méthodologique, révision et édition
B. C. — Analyse documentaire
A. F. — Révision et édition
L. W. — Révision et édition
Intérêts concurrentiels
Aucun.
Remerciements
Les auteurs souhaitent remercier les partenaires de surveillance provinciaux et territoriaux, la section des Couvertures vaccinales et systèmes d'information, le Programme de surveillance de l'efficacité des vaccins, l'équipe de la Science des risques en santé publique/Laboratoire national de microbiologie, l'Équipe d'intégration des données et l'Équipe de surveillance de la COVID-19 de l'Agence de santé publique du Canada. L'Agence a inclus les auteurs suivants par équipe :
Équipe de surveillance de la COVID-19, Centre de l'immunisation et des maladies respiratoires infectieuses : F. Bang, S. Buckrell, N. Lapczak, S. Merali, J. Mielczarek, et L. Whitmore.
Laboratoire national/scientifique des risques pour la santé publique : M. Li
Équipe du Système d'information et de couverture vaccinale, Centre de surveillance de l'immunisation : B. Ho Mi Fane, D. Joy-Baysac, V. Lavergne, A. Maquiling et J. Rotondo.
Programme de surveillance de l'efficacité des vaccins, Centre de surveillance de l'immunisation : A. Fall et B. Cheng.
Financement
Ces travaux ont été soutenus par l'Agence de la santé publique du Canada.
Matériel supplémentaire
Ces documents sont accessibles dans le fichier « Matériel supplémentaire ».
Figure S1 : Ligne du temps des évènements, pertinents, relatifs au programme de vaccination au Canada pour les 12 ans et plus, de décembre 2020 à août 2021
Figure S2 : Distribution du pourcentage cumulatif des personnes « entièrement vaccinés » selon le mois de la dernière dose et la province/le territoire, du 1er janvier 2021 au 14 août 2021
Figure S3 : Description des cas inclus dans analyse
Tableau S1 : Nombre et pourcentage des 12 ans et plus qui étaient « entièrement vaccinés » selon la province ou le territoire, le groupe d'âge et le sexe au Canada, en date du 14 août 2021
Tableau S2 : Nombre et pourcentage des 12 ans et plus qui étaient « entièrement vaccinés » selon l'intervalle entre les doses, le mois de la dernière dose et les vaccins reçus au Canada, en date du 14 août 2021
Tableau S3 : Effets prédits des variables incluses dans le modèle 1 sur la probabilité de devenir un cas signalé de COVID-19, après ajustement pour toutes les autres variables
Figure S4 : Effet du sexe sur la probabilité prédite que des personnes « entièrement vaccinés » deviennent un cas signalé de COVID-19 dans le modèle principal 1, et le modèle 2 (conditionnel au statut de vaccination complète)
Tableau S4 : Effets prédits des variables incluses dans le modèle 2 sur la probabilité de devenir un cas signalé de COVID-19, après ajustement pour toutes les autres variables
Références
- Note de bas de page 1
-
Agence de santé publique du Canada. Rapport de l'administratrice en chef de la santé publique du Canada sur l'état de la santé publique au Canada 2020. Du risque à la résilience : Une approche axée sur l'équité concernant la COVID-19. Ottawa, ON : ASPC; 2020. [Consulté le 17 juin 2022]. https://www.canada.ca/fr/sante-publique/organisation/publications/rapports-etat-sante-publique-canada-administrateur-chef-sante-publique/du-risque-resilience-approche-equite-covid-19.html
- Note de bas de page 2
-
World Health Organization. Statement on the second meeting of the International Health Regulations (2005) Emergency Committee regarding the outbreak of novel coronavirus (2019-nCoV). Geneva (CH): WHO; January 30, 2020. [Consulté le 17 juin 2022]. https://web.archive.org/web/20210815071616/https://www.who.int/news/item/30-01-2020-statement-on-the-second-meeting-of-the-international-health-regulations-%282005%29-emergency-committee-regarding-the-outbreak-of-novel-coronavirus-%282019-ncov%29
- Note de bas de page 3
-
Agence de santé publique du Canada. Plan de vaccination du Canada contre la COVID-19 : sauver des vies et protéger les moyens de subsistance. Ottawa, ON : ASPC; 2020. [Consulté le 17 juin 2022]. https://www.canada.ca/fr/sante-publique/services/maladies/2019-nouveau-coronavirus/reponse-canada/plan-vaccination-canada-contre-covid-19.html
- Note de bas de page 4
-
Agence de santé publique du Canada. Comité consultatif national de l'immunisation (CCNI). Résumé de la déclaration du Comité consultatif national de l'immunisation du 17 juin 2021. Ottawa, ON : ASPC; 2021. [Consulté le 28 sept. 2022]. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/recommandations-utilisation-vaccins-covid-19/resume-declaration-17-juin-2021.html
- Note de bas de page 5
-
Agence de santé publique du Canada. Vaccination contre la COVID-19 : Manière de se faire vacciner. Ottawa, ON : ASPC; 2022. [Consulté le 17 juin 2022]. https://www.canada.ca/fr/sante-publique/services/maladies/maladie-coronavirus-covid-19/vaccins/comment-vacciner.html
- Note de bas de page 6
-
Andrews N, Tessier E, Stowe J, Gower C, Kirsebom F, Simmons R, Gallagher E, Thelwall S, Groves N, Dabrera G, Myers R, Campbell CN, Amirthalingam G, Edmunds M, Zambon M, Brown K, Hopkins S, Chand M, Ladhani SN, Ramsay M, Lopez Bernal J. Duration of protection against mild and severe disease by covid-19 vaccines. N Engl J Med 2022;386(4):340–50. https://doi.org/10.1056/NEJMoa2115481
- Note de bas de page 7
-
Agence de santé publique du Canada. Vaccination contre la COVID-19 au Canada. Ottawa, ON : ASPC; 2023. [Consulté le 17 juin 2022]. https://sante-infobase.canada.ca/covid-19/vaccins-distribues/
- Note de bas de page 8
-
Harris JE. COVID-19 Incidence and hospitalization during the delta surge were inversely related to vaccination coverage among the most populous U.S. Counties. Health Policy Technol 2022;11(2):100583. https://doi.org/10.1016/j.hlpt.2021.100583
- Note de bas de page 9
-
Chemaitelly H, Tang P, Hasan MR, AlMukdad S, Yassine HM, Benslimane FM, Al Khatib HA, Coyle P, Ayoub HH, Al Kanaani Z, Al Kuwari E, Jeremijenko A, Kaleeckal AH, Latif AN, Shaik RM, Abdul Rahim HF, Nasrallah GK, Al Kuwari MG, Al Romaihi HE, Butt AA, Al-Thani MH, Al Khal A, Bertollini R, Abu-Raddad LJ. Waning of BNT162b2 Vaccine Protection against SARS-CoV-2 Infection in Qatar. N Engl J Med 2021;385(24):e83. https://doi.org/10.1056/NEJMoa2114114
- Note de bas de page 10
-
Cerqueira-Silva T, Oliveira VA, Boaventura VS, Pescarini JM, Júnior JB, Machado TM, Flores-Ortiz R, Penna GO, Ichihara MY, de Barros JV, Barreto ML, Werneck GL, Barral-Netto M. Influence of age on the effectiveness and duration of protection of Vaxzevria and CoronaVac vaccines: A population-based study. Lancet Reg Health Am 2022;6:100154. https://doi.org/10.1016/j.lana.2021.100154
- Note de bas de page 11
-
Goldberg Y, Mandel M, Bar-On YM, Bodenheimer O, Freedman L, Haas EJ, Milo R, Alroy-Preis S, Ash N, Huppert A. Waning immunity after the BNT162B2 vaccine in Israel. N Engl J Med 2021;385(24):e85. https://doi.org/10.1056/NEJMoa2114228
- Note de bas de page 12
-
Feikin DR, Higdon MM, Abu-Raddad LJ, Andrews N, Araos R, Goldberg Y, Groome MJ, Huppert A, O'Brien KL, Smith PG, Wilder-Smith A, Zeger S, Deloria Knoll M, Patel MK. Duration of effectiveness of vaccines against SARS-CoV-2 infection and COVID-19 disease: results of a systematic review and meta-regression. Lancet 2022;399(10328):924–44. https://doi.org/10.1016/S0140-6736(22)00152-0
- Note de bas de page 13
-
Glatman-Freedman A, Bromberg M, Dichtiar R, Hershkovitz Y, Keinan-Boker L. The BNT162b2 vaccine effectiveness against new COVID-19 cases and complications of breakthrough cases: A nation-wide retrospective longitudinal multiple cohort analysis using individualised data. EBioMedicine 2021;72:103574. https://doi.org/10.1016/j.ebiom.2021.103574
- Note de bas de page 14
-
Andrews N, Stowe J, Kirsebom F, Toffa S, Sachdeva R, Gower C, Ramsay M, Lopez Bernal J. Effectiveness of COVID-19 booster vaccines against COVID-19-related symptoms, hospitalization and death in England. Nat Med 2022;28(4):831–7. https://doi.org/10.1038/s41591-022-01699-1
- Note de bas de page 15
-
Lauring AS, Tenforde MW, Chappell JD, Gaglani M, Ginde AA, McNeal T, Ghamande S, Douin DJ, Talbot HK, Casey JD, Mohr NM, Zepeski A, Shapiro NI, Gibbs KW, Files DC, Hager DN, Shehu A, Prekker ME, Erickson HL, Exline MC, Gong MN, Mohamed A, Johnson NJ, Srinivasan V, Steingrub JS, Peltan ID, Brown SM, Martin ET, Monto AS, Khan A, Hough CL, Busse LW, Ten Lohuis CC, Duggal A, Wilson JG, Gordon AJ, Qadir N, Chang SY, Mallow C, Rivas C, Babcock HM, Kwon JH, Halasa N, Grijalva CG, Rice TW, Stubblefield WB, Baughman A, Womack KN, Rhoads JP, Lindsell CJ, Hart KW, Zhu Y, Adams K, Schrag SJ, Olson SM, Kobayashi M, Verani JR, Patel MM, Self WH. Influenza and Other Viruses in the Acutely Ill (IVY) Network. Clinical severity and mRNA effectiveness for Omicron, Delta, and Alpha Sars-COV-2 variants in the United States: prospective observational study. BMJ 2022;376:e069761. https://doi.org/10.1136/bmj-2021-069761
- Note de bas de page 16
-
Tan SH, Pung R, Wang LF, Lye DC, Ong B, Cook AR, Tan KB. Association of homologous and heterologous vaccine boosters with COVID-19 incidence and severity in Singapore. JAMA 2022;327(12):1181–2. https://doi.org/10.1001/jama.2022.1922
- Note de bas de page 17
-
Agence de santé publique du Canada. Mise à jour sur l'épidémiologie de la COVID-19: Cas signalés après la vaccination. Ottawa, ON : ASPC; 2022. [Consulté le 17 juin 2022]. https://sante-infobase.canada.ca/covid-19/cas-apres-vaccination.html
- Note de bas de page 18
-
Mizrahi B, Lotan R, Kalkstein N, Peretz A, Perez G, Ben-Tov A, Chodick G, Gazit S, Patalon T. Correlation of SARS-CoV-2-breakthrough infections to time-from-vaccine. Nat Commun 2021;12(1):6379. https://doi.org/10.1038/s41467-021-26672-3
- Note de bas de page 19
-
Statistique Canada. Estimations démographiques trimestrielles (EDT). Ottawa, ON: StatCan; juin 2022. [Consulté le 17 juin 2022]. https://www23.statcan.gc.ca/imdb/p2SV_f.pl?Function=getSurvey&SDDS=3601
- Note de bas de page 20
-
Agence de santé publique du Canada. Définition nationale de cas : Maladie à coronavirus (COVID-19). Ottawa, ON : ASPC; 2022 [Consulté le 17 juin 2022]. https://www.canada.ca/fr/sante-publique/services/maladies/2019-nouveau-coronavirus/professionnels-sante/definition-nationale-cas.html
- Note de bas de page 21
-
Agence de santé publique du Canada. Mise à jour sur l'épidémiologie de la COVID-19: Mises à jour clés. Ottawa, ON : ASPC; Jan 2023. [Consulté le 28 sept. 2022]. https://sante-infobase.canada.ca/covid-19/
- Note de bas de page 22
-
Agence de santé publique du Canada. Comité consultatif national de l'immunisation (CCNI). Comité consultatif national de l'immunisation (CCNI) : Résumé de la déclaration sur l'allongement des intervalles entre les doses du 7 avril 2021. Ottawa, ON : ASPC; avril 2021. [Consulté le 28 sept. 2022]. https://www.canada.ca/fr/sante-publique/services/immunisation/comite-consultatif-national-immunisation-ccni/covid-19-resume-declaration-allongement-intervalles-entre-doses.html
- Note de bas de page 23
-
Detsky AS, Bogoch II. COVID-19 in Canada: Experience and Response to Waves 2 and 3. JAMA 2021;326(12):1145–6. https://doi.org/10.1001/jama.2021.14797
- Note de bas de page 24
-
Shah SA, Robertson C, Rudan I, Murray JL, McCowan C, Grange Z, Buelo A, Sullivan C, Simpson CR, Ritchie LD, Sheikh A. BNT162b2 and ChAdOx1 nCoV-19 vaccinations, incidence of SARS-CoV-2 infections and COVID-19 hospitalisations in Scotland in the Delta era. J Glob Health 2022;12:05008. https://doi.org/10.7189/jogh.12.05008
- Note de bas de page 25
-
Pouwels KB, Pritchard E, Matthews PC, Stoesser N, Eyre DW, Vihta KD, House T, Hay J, Bell JI, Newton JN, Farrar J, Crook D, Cook D, Rourke E, Studley R, Peto TE, Diamond I, Walker AS. Effect of Delta variant on viral burden and vaccine effectiveness against new SARS-CoV-2 infections in the UK. Nat Med 2021;27(12):2127–35. https://doi.org/10.1038/s41591-021-01548-7
- Note de bas de page 26
-
Agence de santé publique du Canada. Infections par la COVID-19 parmi les travailleurs de la santé et les autres personnes travaillant dans les établissements de soins de santé. Ottawa, ON : ASPC; mars 2022. [Consulté le 17 juin 2022]. https://www.canada.ca/fr/sante-publique/services/maladies/maladie-coronavirus-covid-19/recherches-donnees-epidemiologiques-economiques/infections-travailleurs-sante-autres-personnes-travaillant-etablissements-soins-sante.html
- Note de bas de page 27
-
Sriharan A, Ratnapalan S, Tricco AC, Lupea D, Ayala AP, Pang H, Lee DD. Occupational Stress, Burnout, and Depression in Women in Healthcare During COVID-19 Pandemic: Rapid Scoping Review. Front Glob Womens Health 2020;1:596690. https://doi.org/10.3389/fgwh.2020.596690
- Note de bas de page 28
-
Israel A, Merzon E, Schäffer AA, Shenhar Y, Green I, Golan-Cohen A, Ruppin E, Magen E, Vinker S. Elapsed time since BNT162b2 vaccine and risk of SARS-CoV-2 infection: test negative design study. BMJ 2021;375:e067873. https://doi.org/10.1136/bmj-2021-067873
- Note de bas de page 29
-
Naleway AL, Groom HC, Crawford PM, Salas SB, Henninger ML, Donald JL, Smith N, Thompson MG, Blanton LH, Bozio CH, Azziz-Baumgartner E. Incidence of SARS-CoV-2 Infection, Emergency Department Visits, and Hospitalizations Because of COVID-19 Among Persons Aged ≥12 Years, by COVID-19 Vaccination Status - Oregon and Washington, July 4-September 25, 2021. MMWR Morb Mortal Wkly Rep 2021;70(46):1608–12. https://doi.org/10.15585/mmwr.mm7046a4
- Note de bas de page 30
-
Fabiani M, Puopolo M, Filia A, Sacco C, Mateo-Urdiales A, Spila Alegiani S, Del Manso M, D'Ancona F, Vescio F, Bressi M, Petrone D, Spuri M, Rota MC, Massari M, Da Cas R, Morciano C, Stefanelli P, Bella A, Tallon M, Proietti V, Siddu A, Battilomo S, Palamara AT, Popoli P, Brusaferro S, Rezza G, Riccardo F, Menniti Ippolito F, Pezzotti P. Effectiveness of an mRNA vaccine booster dose against SARS-CoV-2 infection and severe COVID-19 in persons aged ≥60 years and other high-risk groups during predominant circulation of the delta variant in Italy, 19 July to 12 December 2021. Expert Rev Vaccines 2022;21(7):975–82. https://doi.org/10.1080/14760584.2022.2064280
- Note de bas de page 31
-
Chung H, He S, Nasreen S, Sundaram ME, Buchan SA, Wilson SE, Chen B, Calzavara A, Fell DB, Austin PC, Wilson K, Schwartz KL, Brown KA, Gubbay JB, Basta NE, Mahmud SM, Righolt CH, Svenson LW, MacDonald SE, Janjua NZ, Tadrous M, Kwong JC; Canadian Immunization Research Network (CIRN) Provincial Collaborative Network (PCN) Investigators. Effectiveness of BNT162b2 and mRNA-1273 covid-19 vaccines against symptomatic SARS-CoV-2 infection and severe covid-19 outcomes in Ontario, Canada: test negative design study. BMJ 2021;374:n1943. https://doi.org/10.1136/bmj.n1943
- Note de bas de page 32
-
Heftdal LD, Schultz M, Lange T, Knudsen AD, Fogh K, Hasselbalch RB, Linander CB, Kallemose T, Bundgaard H, Grønbæk K, Valentiner-Branth P, Iversen K, Nielsen SD. Incidence of Positive Severe Acute Respiratory Syndrome Coronavirus Polymerase Chain Reaction After Coronavirus Disease 2019 Vaccination With up to 8 Months of Follow-up: Real-life Data From the Capital Region of Denmark. Clin Infect Dis 2022;75(1):e675–82. https://doi.org/10.1093/cid/ciac012
- Note de bas de page 33
-
Britton A, Fleming-Dutra KE, Shang N, Smith ZR, Dorji T, Derado G, Accorsi EK, Ajani UA, Miller J, Schrag SJ, Verani JR. Association of COVID-19 Vaccination With Symptomatic SARS-CoV-2 Infection by Time Since Vaccination and Delta Variant Predominance. JAMA 2022;327(11):1032–41. https://doi.org/10.1001/jama.2022.2068
- Note de bas de page 34
-
de Michelena P, Torres I, Albert E, Bracho A, González-Candelas F, Navarro D. Impact of time elapsed since full vaccination on SARS-CoV-2 RNA load in Delta-variant breakthrough COVID-19. J Infect 2022;84(4):579–613. https://doi.org/10.1016/j.jinf.2022.01.006
- Note de bas de page 35
-
Skowronski DM, Febriani Y, Ouakki M, Setayeshgar S, El Adam S, Zou M, Talbot D, Prystajecky N, Tyson JR, Gilca R, Brousseau N, Deceuninck G, Galanis E, Fjell CD, Sbihi H, Fortin E, Barkati S, Sauvageau C, Naus M, Patrick DM, Henry B, Hoang LM, De Wals P, Garenc C, Carignan A, Drolet M, Jassem AN, Sadarangani M, Brisson M, Krajden M, De Serres G. Two-dose severe acute respiratory syndrome coronavirus 2 vaccine effectiveness with mixed schedules and extended dosing intervals: test-negative design studies from British Columbia and Quebec, Canada. Clin Infect Dis 2022;75(11):1980–92. https://doi.org/10.1093/cid/ciac290
- Note de bas de page 36
-
Centers for Disease Control and Prevention. CDC COVID-19 Study Shows mRNA Vaccines Reduce Risk of Infection by 91 Percent for Fully Vaccinated People. Atlanta, GA; CDC; June 2021 [Consulté le 4 oct. 2022]. https://www.cdc.gov/media/releases/2021/p0607-mrna-reduce-risks.html#:~:text=Once%20fully%20vaccinated%2C%20participants'%20risk,included%20symptomatic%20
and%20asymptomatic%20infections - Note de bas de page 37
-
Britton A, Jacobs Slifka KM, Edens C, Nanduri SA, Bart SM, Shang N, Harizaj A, Armstrong J, Xu K, Ehrlich HY, Soda E, Derado G, Verani JR, Schrag SJ, Jernigan JA, Leung VH, Parikh S. Effectiveness of the Pfizer-BioNtech Covid-19 Vaccine among Residents of Two Skilled Nursing Facilities Experiencing Covid-19 Outbreaks - Connecticut, December 2020–February 2021. MMWR Morbid Mortal Wkly Rep. 2021;70(11):396–401. https://www.cdc.gov/mmwr/volumes/70/wr/mm7011e3.htm
- Note de bas de page 38
-
European Centre for Disease Prevention and Control. Partial COVID-19 vaccination, vaccination following SARS-COV-2 infection and heterologous vaccination schedule: Summary of evidence. Solna (SE); ECDC; July 2021. [Consulté le 4 oct. 2022]. https://www.ecdc.europa.eu/en/publications-data/partial-covid-19-vaccination-summary

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International
Détails de la page
- Date de modification :